Withania Somnifera (Витания Сомнифера), обычно называемая Ашвагандой, является целебной травой, часто используемой в Аюрведе, традиционном методе медицины, практикуемом в Индии. Ашваганда продемонстрировала способность оказывать ряд противовоспалительных, противоопухолевых, антиоксидантных, антистрессовых, антидиабетических и кардиопротекторных эффектов [1]. Текущие исследования направлены на выделение и усиление действия этого соединения, чтобы направить его полезные свойства на участки тела, поврежденные воспалением и окислительным стрессом.
1) Было обнаружено, что лечение ашвагандой предотвращает повышение перекисного окисления липидов, вызванное липополисахаридом и пептидогликаном, вводимыми в дозах, имитирующих биологические эффекты повседневных стрессоров.
2) Было обнаружено, что лечение ашвагандой улучшает двигательную активность и когнитивные функции, уровень аммиака, гистопатологические изменения в мозге и печени, а также уровни MDA, GS, iNOS, GSH, Nrf2 и HO-1 в мозге и печени, а также снижает экспрессию p38, экспрессию мРНК ERK1/2, NF-kB и TNF-альфа.
1) Известно, что липополисахарид и пептидогликан изменяют фармакокинетику перорально вводимых лекарств и действуют в организме как внутренние стрессоры. Присутствие этих соединений связано с повышенным перекисным окислением липидов и образованием свободных радикалов, что приводит к повреждению клеток. Исследователь Джаян Н. Дули и др. изучали влияние ашваганды на перекисное окисление липидов, вызванное липополисахаридом и пептидогликаном у кроликов и мышей [2].
Для этого исследования использовались самцы бельгийских кроликов-альбиносов весом 2,5–3,0 кг каждый и мыши штамма Hindustan antibiotic весом 20–30 граммов каждая. Все испытуемые содержались в относительно влажном помещении с кондиционером и содержались в цикле 10 часов света/14 часов темноты. Кролики получали стандартную гранулированную диету с водой и травой лейцерна, предоставляемой ad libitum, а мыши получали стандартную гранулированную диету с доступом к воде ad libitum.
0,2 мкг/кг липополисахарида или 100 мкг/кг пептидогликана растворяли в физиологическом растворе и вводили в краевую ушную вену кроликов и в хвостовую вену мышей. 100 мг/кг ашваганды перорально вводили одной группе кроликов, получавших липополисахарид, одной группе мышей, получавших липополисахарид, одной группе кроликов, получавших пептидогликан, и одной группе мышей, получавших пептидогликан. Все виды лечения вводились подопытным животным одновременно, в то время как контрольная группа получала 2% аравийской камеди перорально и физиологический раствор внутривенно. Образцы крови собирали у испытуемых путем сердечной пункции до начала лечения, а также через 1, 2, 4, 6, 8, 10 и 24 часа после лечения [2].
Перекисное окисление липидов оценивалось путем сбора образцов крови у всех испытуемых и смешивания их с додецилсульфатом натрия, ацетатным буфером и водным раствором. Смесь нагревалась в течение 60 минут, и после охлаждения красный пигмент экстрагировался с использованием н-бутанола:пиридина. Тетраметоксипропан использовался в качестве внешнего стандарта, а перекисное окисление липидов выражалось с использованием коэффициента экстинкции в эквивалентах малонового диальдегида. Статистические различия между полученными результатами определялись с помощью t-критерия Стьюдента [2].
2) Исследовательская группа Халила и др. изучает способность Ашваганды снижать быстрое развитие гепатоцеллюлярного повреждения и энцефалопатии, связанной с острой печеночной недостаточностью, поскольку она связана с нейропсихиатрической дисфункцией, характеризующейся когнитивными дефицитами, нарушением сознания и в конечном итоге смертью. Для целей данного исследования были использованы 28 взрослых самок крыс Wistar весом 150-180 граммов каждая. Крысы содержались в стандартных лабораторных условиях с неограниченным доступом к коммерческой диете и воде и им позволяли акклиматизироваться к окружающей среде до начала экспериментального тестирования [3].
Каждая крыса была случайным образом распределена в одну из 4 групп по 7 человек в каждой. Группа 1 была отрицательной контрольной группой, включающей нормальных крыс, которым вводили 2 мл/кг воды через зонд в течение 30 дней. Группа 2 была положительной контрольной группой, включающей крыс, которым внутрибрюшинно вводили 350 мг/кг тиоацетамида (ТАА) на 30-й день эксперимента. Группа 3 включала крыс, которым предварительно вводили 200 мг/кг Ашваганды через зонд в течение 30 дней, а затем вводили 350 мг/кг ТАА на 30-й день. Группа 4 включала крыс, которым предварительно вводили 400 мг/кг Ашваганды через зонд в течение 30 дней, а затем вводили 350 мг/кг ТАА на 30-й день. Поведенческие тесты, проведенные испытуемыми в этом эксперименте, включали тест «Открытое поле», тест с Y-образным лабиринтом, модифицированный приподнятый крестообразный лабиринт и тест на распознавание новых объектов; Поведенческое тестирование проводилось с 31-го по 35-й день с 9:00 до 15:00.
Сначала проводился тест открытого поля; самок крыс помещали в аппарат открытого поля, чтобы в ходе исследования можно было изучить их локомоторную активность и исследовательское поведение. Аппарат открытого поля состоял из квадратной деревянной коробки с полом, разделенным на 16 равных квадратов. После того, как крыс осторожно помещали в один из углов коробки, им позволяли исследовать в течение 3 минут, в то время как общее количество переходов и активности вставания на задние лапы оценивалось как репрезентативность локомоции и исследования соответственно. Между каждым испытанием аппарат очищали спиртом и давали ему высохнуть на воздухе перед началом следующего сеанса тестирования [3].
Следующей поведенческой оценкой был тест Y-лабиринта, который наблюдал за пространственной рабочей памятью у крыс с индуцированным гепатоцеллюлярным повреждением и энцефалопатией. Крыс помещали в один угол аппарата Y-лабиринта и позволяли исследовать в течение 5 минут, в то время как исследователи наблюдали и регистрировали количество входов в рукава и спонтанное чередующееся поведение. Измеренные параметры служат представлением как двигательной активности, так и естественной способности крыс различать различные секции лабиринта. За тестами открытого поля и Y-лабиринта следовал модифицированный тест приподнятого крестообразного лабиринта. Этот лабиринт использовался для оценки долговременной пространственной памяти с использованием деревянного приподнятого крестообразного лабиринта с двумя открытыми рукавами и двумя закрытыми рукавами, соединенными центральной платформой. Процедуры модифицированного теста приподнятого крестообразного лабиринта включают две различные фазы, которые проходят с интервалом в 24 часа [3].
Первая фаза определяется как фаза приобретения, когда испытуемые помещаются на один конец открытого рукава лицом к внешней стороне рукава. Затем исследователь регистрировал и рассчитывал количество времени, которое требуется крысе, чтобы переместиться в один из закрытых рукавов лабиринта. Это количество времени, которое требовалось, называлось задержкой переноса-1. Затем испытуемым разрешалось исследовать закрытый рукав в течение 30 секунд. Если через 90 секунд животное не выходило из открытого рукава, чтобы исследовать закрытый рукав, исследователи мягко подталкивали его в закрытый рукав и позволяли исследовать в течение 10 секунд. Вторая фаза модифицированного приподнятого крестообразного лабиринта была фазой тестирования, где задержка переноса-2 измерялась путем оценки того, сколько времени требовалось животному, чтобы достичь одного из закрытых рукавов до того, как истекло отведенное время в 90 секунд.
Заключительным поведенческим экзаменом был тест на распознавание новых объектов, который оценивал гиппокамп-зависимую память и когнитивные нарушения, связанные с гепатоцеллюлярным повреждением и энцефалопатией. Тест включал деревянный квадратный ящик, который был задействован в трех различных тестовых испытаниях, которые проводились с интервалом в 24 часа. Первым испытанием было испытание привыкания, когда крыс помещали внутрь аппарата и позволяли им ознакомиться в течение 3 минут. Вторым испытанием было испытание на приобретение, когда крысам позволяли исследовать и знакомиться с двумя идентичными объектами в коробке в течение 5 минут. Для этой цели данного исследования идентичными объектами были две гантели весом 1,0 кг. Третьим испытанием было испытание на припоминание, когда крысам позволяли исследовать и знакомиться с одним знакомым объектом, гантелью весом 1,0 кг, и новым объектом, бутылкой с водой объемом 1 л, в коробке в течение 5 минут. Исследовательская группа наблюдала исследовательскую активность животных, которая определялась как обнюхивание и прикосновение к объектам в коробке. Важно отметить, что лазание животных по объектам не считалось исследовательской деятельностью. На основе собранных данных был рассчитан коэффициент дискриминации и индекс распознавания [3].
Через 24 часа после проведения поведенческого тестирования были собраны образцы блота из ретроорбитального сплетения и оставлены для свертывания, после чего проведено 10-минутное центрифугирование для отделения сыворотки. Затем крысы были подвергнуты эвтаназии, а образцы из печени и мозга были собраны и сохранены для дальнейшей экспрессии генов и биохимических анализов. Различные проведенные биохимические оценки включали определение сывороточных уровней аммиака, аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), щелочной фосфатазы (ЩФ), альбумина и общего уровня белка. Кроме того, гомогенаты из тканей печени и мозга использовались для количественного определения уровней восстановленного глутатиона и перекисного окисления липидов, в то время как анализ ELISA количественно определял количество глутаминсинтетазы (ГС), Nrf2, гем-оксигеназы-1 (HO-1) и индуцируемой синтазы оксида азота (iNOS) с использованием гомогенатов из тканей печени и мозга.
Гистопатологические и иммуногистохимические исследования проводились путем фиксации образцов печени и мозга в формалине с последующей подготовкой в соответствии с протоколом и заливкой в парафин. Срезы толщиной 5 мкм были нарезаны и окрашены гематоксилином, эозином и трихромом по Массону для того, чтобы окрашенные слайды можно было исследовать с помощью светового микроскопа. Образцам печени была присвоена гистологическая оценка от 0 до 3 в зависимости от тяжести воспаления, регионального некроза, обширного некроза и фиброза, присутствующих в образцах. Срезы мозга также получили гистологическую оценку по шкале от 0 до 3 в зависимости от тяжести нейронального отека, нейронального некроза и инфильтрации астроцитов в образцах [3].
1) Известно, что эндотоксины, такие как липополисахарид и пептидогликан, вызывают различные нейроэндокринные физиологические изменения. Это происходит из-за цепочки клеточных событий, включающих активацию цитокинов, таких как интерлейкины и факторы некроза опухоли, которые тесно связаны с воспалением и различными патологическими особенностями в организме. Целью исследования, проведенного Дули, была оценка того, как введение ашваганды влияет на перекисное окисление липидов, вызванное липополисахаридом и пептидогликаном в модели исследования на животных, состоящей из кроликов и мышей. Важно отметить, что липополисахарид и пептидогликан давались испытуемым в дозах, которые имитировали условия стрессовых ситуаций повседневной жизни. Было подтверждено, что перекисное окисление липидов происходило, когда оба стрессорных соединения вводились животным внутривенно [2].
Было отмечено различие во времени начала индуцированного перекисного окисления липидов каждым соединением; пиковое воздействие липополисахарида достигалось через 2-6 часов после введения, тогда как пиковое воздействие пептидогликана достигалось через 1 час после введения. После введения липополисахарида наблюдалось значительное увеличение перекисного окисления липидов как у кроликов, так и у мышей. Когда ашваганда была доставлена животным в то же время, повышение уровня перекисного окисления липидов было значительно предотвращено соединением. Кроме того, было обнаружено, что введение пептидогликана приводит к увеличению перекисного окисления липидов как у кроликов, так и у мышей. Было показано, что одновременное введение ашваганды значительно предотвращает это повышение уровня перекисного окисления липидов [2].
Также было обнаружено, что ашваганда подавляет повышенное перекисное окисление липидов, воздействуя на процесс удаления свободных радикалов, а не на систему глутатиона. Это было важным замечанием, учитывая, что система глутатиона является одной из основных физиологических антиоксидантных систем в организме. В целом, исследование пришло к выводу, что прием ашваганды предотвращает повышенное перекисное окисление липидов, вызванное наличием липополисахарида и пептидогликана [2].
2) Результаты исследования, проведенного Халилом и др., показали, что у крыс, отравленных ТАА, которые прошли тест открытого поля, наблюдалось значительное снижение количества переходов в другие квадранты, а также частоты задних стойк в качестве измерения локомоции и исследовательского поведения соответственно. Когда ашваганда вводилась животным в дозах 200 мг/кг и 400 мг/кг, как исследовательское поведение, так и активность локомоции значительно возросли по сравнению с крысами, отравленными ТАА. Важно отметить, что, хотя обе дозы были эффективными, наблюдаемое поведение и активность были улучшены в большей степени у животных, получавших 400 мг/кг ашваганды [3].
Затем крыса прошла тест Y-лабиринта в качестве измерения пространственной рабочей памяти. Результаты показали, что животные, отравленные ТАА, испытали значительно меньшее количество чередований по сравнению с контрольными группами крыс. Когда животные были предварительно обработаны Ашвагандой, те, кому была введена доза 400 мг/кг, испытали заметное повышение спонтанных чередований по сравнению с группой, отравленной ТАА. Однако важно отметить, что не было никаких существенных изменений в спонтанных чередованиях у крыс, которым была введена 200 мг/кг Ашваганды. С точки зрения частоты, с которой животные входили в различные рукава лабиринта, было показано, что как дозы 200 мг/кг, так и 400 мг/кг предварительной обработки Ашваганды значительно увеличили частоту входов в рукава.
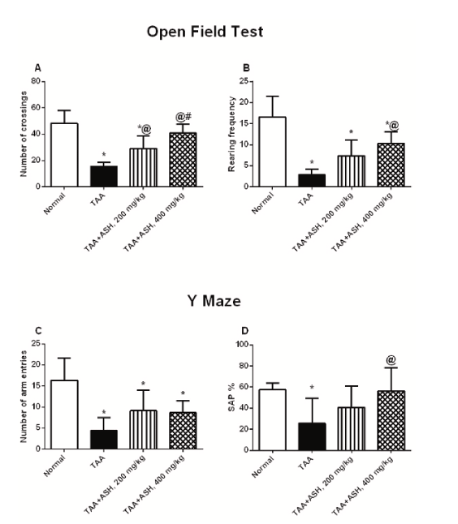
Рисунок 1: Изменения в A) количестве переходов и B) частоте вставания на задние лапы во время теста «открытое поле», а также изменения в C) количестве входов в рукава и D) проценте спонтанного чередования во время теста с Y-лабиринтом, измеренные в экспериментальных группах.
Модифицированный приподнятый крестообразный лабиринт был пройден испытуемыми следующим образом, чтобы оценить долговременную память животных. Результаты показывают, что не было никаких существенных различий в результатах, полученных от разных экспериментальных групп с точки зрения измерения задержки переноса-1. Для измерения задержки переноса-2 крысы, отравленные ТАА, показали увеличенное количество времени, необходимое для перехода в закрытый рукав лабиринта из открытого, по сравнению с контрольной группой. Когда ашваганда вводилась животным в дозах 200 мг/кг и 400 мг/кг, количество времени, необходимое животному для перехода в закрытый рукав лабиринта, было значительно короче по сравнению с крысами, отравленными ТАА. Важно отметить, что, хотя обе дозы были эффективными, задержка переноса-2 была снижена в большей степени у животных, получавших 400 мг/кг ашваганды [3].
Тест на распознавание новых объектов был последним поведенческим обследованием, которое проходили крысы для оценки их непространственной рабочей памяти. Не было обнаружено, что зарегистрированное отношение дискриминации претерпело какие-либо существенные изменения между различными экспериментальными группами лечения. У крыс, отравленных ТАА, наблюдалось значительное снижение индекса распознавания по сравнению с группой контрольных крыс. Когда ашваганда вводилась животным в дозах 200 мг/кг и 400 мг/кг, индекс распознавания животных значительно увеличивался по сравнению с крысами, отравленными ТАА. Важно отметить, что, хотя обе дозы были эффективными, индекс распознавания был повышен в большей степени у животных, получавших 400 мг/кг ашваганды.
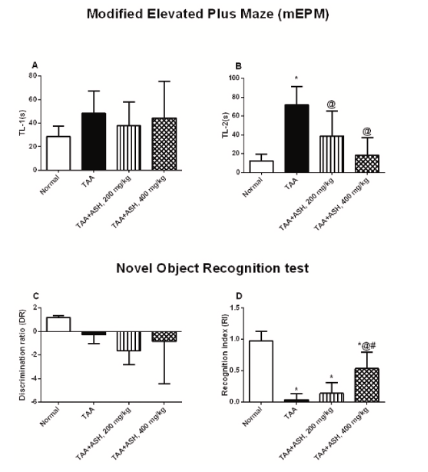
Рисунок 2: Изменения в A) латентном времени-1 и B) латентном времени-2 во время модифицированного приподнятого крестообразного лабиринта, а также изменения в C) коэффициенте дискриминации и D) индексе распознавания во время измерения теста на распознавание новых объектов в экспериментальных группах лечения.
Гепатотоксичность оценивали путем измерения изменений в сывороточных уровнях АЛТ, АСТ и ЩФ. После введения ТАА для интоксикации крыс все сывороточные уровни были повышены, в дополнение к заметному снижению общего уровня белка и альбумина. Все уровни АЛТ, АСТ, ЩФ, общего белка и альбумина были восстановлены до исходных уровней при предварительной обработке дозами ашваганды 200 мг/кг и 400 мг/кг. При этом ткани печени оценивали на предмет наличия повреждений, характеризующихся гистопатологическими изменениями. У животных, которым вводили ТАА, наблюдались заметные гепатоцеллюлярные вакуолярные изменения и обширный некроз, указывающие на интенсивное гистопатологическое повреждение. Кроме того, портальные области были инфильтрированы портальной фиброплазией и мононуклеарными воспалительными клетками, в то время как в печеночной паренхиме обнаруживались синусоидальная дилатация и геморрагические области. Когда животные были предварительно обработаны Ашвагандой в дозе 200 мг/кг, наблюдалось легкое улучшение гистопатологических нарушений печени, отмеченное более низкой степенью фиброплазии, очаговыми областями некроза и ограниченными геморрагическими зонами. Когда животные были предварительно обработаны Ашвагандой в дозе 400 мг/кг, была достигнута нормальная функция печени с признаками очень небольшой фиброплазии [3].
Что касается образцов, собранных из мозговых тканей, у крыс, отравленных TAA, был обнаружен обширный периваскулярный и нейрональный отек с некрозом и нейронной дегенерацией, поражающей различные области мозга. Эти результаты сравниваются с крысами, включенными в контрольную группу, у которых наблюдалась нормальная гистологическая структура различных областей мозга. Когда животные были предварительно обработаны 200 мг/кг Ашваганды до интоксикации TAA, наблюдался только легкий отек и очень мало дегенерирующих нейронов в коре головного мозга. Когда крысы были предварительно обработаны 400 мг/кг Ашваганды до интоксикации TAA, срезы мозга выглядели нормальными, как и в контрольной группе, с только легким отеком, наблюдаемым в полосатом теле [3].
Окислительный стресс измеряли по уровням запасов MDA и GSH в печени и тканях. У крыс, отравленных TAA, наблюдалось заметное повышение уровня MDA, связанное с истощением запасов GSH в печени и мозге по сравнению с контрольной группой крыс. При предварительном лечении 200 мг/кг ашваганды повышенные уровни MDA регулировались и снижались, а содержание GHS в печени и мозге восполнялось, в то время как предварительное лечение 400 мг/кг ашваганды, как было показано, усиливало антиоксидантную активность. Повышенную антиоксидантную активность дополнительно оценивали путем измерения уровней Nrf2 и HO-1; у крыс, отравленных TAA, наблюдалось значительное снижение этих маркеров в печени и мозге, однако предварительное лечение 200 мг/кг ашваганды значительно повышало уровни Nrf2 и HO-1, в то время как 400 мг/кг восстанавливали их до исходного уровня [3].
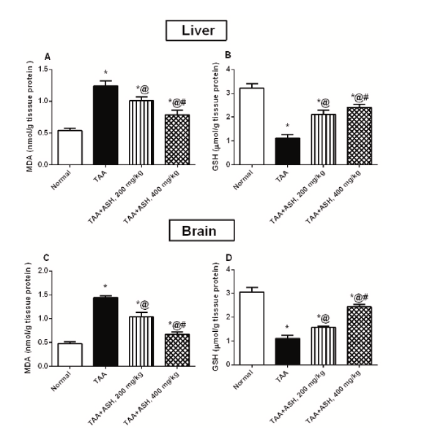
Рисунок 3: Изменения A) MDA в печени, B) GSH в печени, C) MDA в мозге и D) GSH в мозге, измеренные в группах экспериментального лечения.
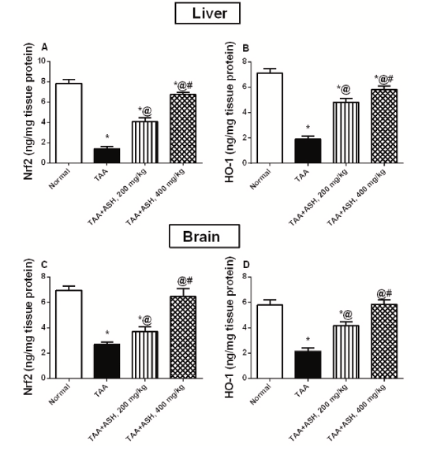
Рисунок 4: Изменения A) Nrf2 в печени, B) HO-1 в печени, C) Nrf2 в мозге и D) HO-1 в мозге, измеренные в группах экспериментального лечения.
[1] Azab KS, Maarouf RE, Abdel-Rafei MK, El Bakary NM, Thabet NM. Withania somnifera (Ashwagandha) root extract counteract acute and chronic impact of γ-radiation on liver and spleen of rats. Hum Exp Toxicol. 2022 Jan-Dec;41:9603271221106344. doi: 10.1177/09603271221106344. PMID: 35656930.
[2] Dhuley JN. Effect of ashwagandha on lipid peroxidation in stress-induced animals. J Ethnopharmacol. 1998 Mar;60(2):173-8. doi: 10.1016/s0378-8741(97)00151-7. PMID: 9582008.
[3] Khalil HMA, Eliwa HA, El-Shiekh RA, Al-Mokaddem AK, Hassan M, Tawfek AM, El-Maadawy WH. Ashwagandha (Withania somnifera) root extract attenuates hepatic and cognitive deficits in thioacetamide-induced rat model of hepatic encephalopathy via induction of Nrf2/HO-1 and mitigation of NF-κB/MAPK signaling pathways. J Ethnopharmacol. 2021 Sep 15;277:114141. doi: 10.1016/j.jep.2021.114141. Epub 2021 Apr 24. PMID: 33905819.